Болезни эндогенной ретровирусной активности
Эндогенные ретроэлементы появляются в геноме человека как следствие вызванных экзогенными ретровирусами эпидемических (эпизоотических — если иметь ввиду наших отдаленных предков) процессов. Однако патология, возникающая в результате их активности уже в геноме человека, не относится учеными к инфекционной, а их распространение по виду Homo sapiens , не считается эпидемией. Причина тут в том, что понимание инфекционных и эпидемических процессов у нас ограничено представлениями о циклических инфекциях (эпидемиях), развивающихся в масштабах времени, воспринимаемых человеком на бытовом уровне. Процессы, растягивающиеся во времени на периоды, выходящие за эти рамки, а тем более начавшиеся в эволюционно предшествующих видах, распадаются на отдельные явления без понимания причинно-следственных связей между ними.
Распространение эндогенных ретроэлементов по геному человека как инфекционный процесс. Во-первых, распространение эндогенных ретроэлементов по геному человека представляет собой размножение и экспансию чуждых для генома генетических структур, попавших в него «из вне»; во-вторых , этот процесс предполагает паразитизм в существовании ретроэлементов — их размножение и распространение по геному человека осуществляется благодаря использованию биохимических ресурсов клетки; в-третьих, вставки ретроэлементов в геном человека приводят к поражению функции органа или ткани, т. е. к болезни.
Также как у микроорганизмов-паразитов, у паразитических ретроэлементов есть свои «экологические ниши», в которых они существуют миллионы лет притом, что виды их хозяев меняются. LTR -ретроэлементы равномерно распределены между AT - и GC -богатыми участками ДНК. Но Alu -элементы «предпочитают» регионы, богатые по GC . Установлена строгая корреляция между плотностью активно транскрибируемых генов (что отражает повышенное содержание GC ) и плотностью Alu -элементов. Отдельные хромосомы, такие как 19-я, содержат большое количество Alu -элементов. Хромосома Y , наоборот, показывает нехарактерно низкую плотность Alu -элементов относительно содержания GC , что связывают с накоплением в этой хромосоме псевдогенов. В противоположность Alu , LINE аккумулируются в регионах, богатых AT [1]. Чем выше генная плотность в каком-то участке хромосомы, тем менее вероятно обнаружение в этом участке HERV или их «следов» виде solo-LTR. Достоверной корреляции фиксации эндогенных ретровирусов со скоростью рекомбинации в конкретном участке хромосомы, не обнаружено [2].
«Новые» ретроэлементы в геноме эукариотов проходят через этапы «взрывов амплификации», когда они активно амплифицируются в течение нескольких десятков миллионов лет. Такой процесс, если его представить в виде графика вне масштаба времени, имеет даже фазу инфекции, которую по аналогии с циклическими инфекционными процессами можно назвать носительством (когда ретроэлементы утрачивают способность к транспозиции, но сохраняются в геноме клетки). На рисунке показана приблизительная шкала времени формирования мобильных элементов в геноме современного вида человека.
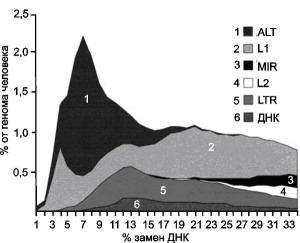
Очередность интеграции мобильных элементов (по времени), обнаруженных в геноме современного вида человека [3]
Общая шкала соответствует периоду эволюционной истории приблизительно в 120 млн. лет, т. е. захватывает период господства рептилий. По оси Х показан процент замен различных вставочных последовательностей относительно их консенсусных последовательностей для генома современного вида человека. По оси Y — процент, который эти ретроэлементы составляют в геноме современного вида человека. Процент замен относительно консенсуса находится в соответствии с возрастом вставок. Чем он больше, тем древнее вставки. Большинство из «недавно» проявивших активность ретроэлементов составляют L 1 и Alu. «Пик» их размножения в эволюционно предшествующих человеку видах имел место 60 млн. лет. В последние несколько десятков миллионов лет наблюдается снижение их активности [3].
Чем более быстро амплифицируется ретроэлемент, тем большее количество копий он образует в геноме хозяина, которые, в свою очередь, вовлекаются в репликацию и транспозицию. Эта тенденция оказывает негативное влияние на жизнеспособность организма вследствие вставочного мутагенеза, неправильных рекомбинационных актов между «рассеянными» по геному ретроэлементами, делеций ДНК и других процессов, вызванных транспозиционной активностью ретроэлементов [3].
Эпидемиология не-LTR-ретроэлементов . Эти древние ретроэлементы составляют до 34 % генома современного вида человека. Два представителя семейства встречаются в геноме человека в очень больших количествах. Это короткие вставочные элементы (SINE) и длинные терминальные вставочные повторы (LINE). Наиболее активны из представителей SINE — Alu- и MIR-повторы; из LINE — автономные L1 и L2 последовательности.
LINE-1 (L1) распространяются по геному человека — одна новая вставка на каждые 10—250 индивидуумов. L1-транспозоны вызывают у людей болезни по разным механизмам, включающим неправильную гомологичную рекомбинацию участков ДНК хромосом; прямые вставки L1 в гены; обеспечение вставок других ретротранспозонов в гены. Перемещение по геному человека L1 вызывает не менее двух видов гемофилии, APC/аденоматозный полипоз кишечника, мышечную дистрофию, бета-глобин/бета-талассемию, RP 2/пигментированный ретинит, CYBB /хронический гранулематоз и др. наследственные болезни [4] .
Продолжается распространение в популяциях современного вида человека Alu-элементов . Их количество в геноме растет, и они встраиваются во все новые сайты с частотой примерно одно новое встраивание на 100—200 новорожденных, увеличивая риск развития патологических процессов, наследуемых по законам Менделя. Среди них нейрофиброматоз, ахолинэстеразомия, гемофилия А и В, семейная гипокальйурическая гиперкальцемия, рак молочной железы, Х-связанная агаммаглобулинемия, Х-связанный тяжелый комбинирован комбинированный иммунодефицит, бранхио-ото-ренальный синдром, болезнь Хангтингтона, синдром Киндлера и др. [5].
Всего же исследования вставок ретротранспозонов, выполненные в последние годы, позволили выявить до 14 генетических болезней, возникших недавно или de novo в результате вставок L1; и, как минимум, 21 болезнь, вызванную вставками Alu .
Эпидемиология LTR-ретроэлементов . Составляют до 8 % генома человека. К ним относятся ретротранспозоны, эндогенные ретровирусы (ERVs), человеческие эндогенные ретровирусы (HERVs) и повторяющиеся элементы эндогенных ретровирусов человека, такие как SINE-R ретропозоны. «Полноразмерность» генома HERV, весьма относительна. HERV представляют собой полиморфизмы, т. е. различные производные от своего экзогенного предка к тому же присутствующие в разных пропорциях в различных популяциях людей. Полиморфизмы делятся на два подтипа.
Полиморфизмы последовательностей — полиморфизмы последовательностей генов HERV, влияющих на функциональную способность их конечных продуктов. Они трудно поддаются идентификации, так как мешает «фон» экспрессирующихся генов сходных эндогенных вирусов.
Вставочный полиморфизм — разное пропорциональное присутствие HERV в различных популяциях людей. Вставочнополиморфные HERV с большей вероятностью вовлечены в патологические процессы, чем HERV, присутствующие у всех представителей вида. Во-первых, они недавно (т. е. в пределах 6 млн лет) вставились в геном современного вида человека (его эволюционных предков) и поэтому могут вызывать разрушение его генов, с которыми интегрировались. Энхансерные элементы ретровирусных LTR могут влиять на экспрессию генов, прилегающих к HERV, даже при наличии некоторой дистанции между ними. Во-вторых, HERV, недавно интегрировавшиеся с геномом человека, с большей вероятностью содержат функциональноактивные гены, способны модулировать клеточную пролиферацию и иммунные реакции. В третьих, их присутствие только у отдельных индивидуумов повышает возможность того, что они усилят свою патогенность таким же образом, как это делают экзогенные ретровирусы [6].
HERV вызывают патологические процессы у людей по следующим механизмам: 1) разрушают гены в участках собственной интеграции; 2) подавляют или стимулируют иммунные ответы; 3) модулируют синтез белков, оказывающих патологическое действие на клетки [6].
* * *
Если изменить масштаб времени с жизни отдельного человека, до жизни его как вида, т. е. до временных интервалов, в которые дают о себе знать эволюционные процессы, то распространение по геному человека эндогенных ретроэлементов можно рассматривать как циклические эпидемии, развивающиеся в рамках сверхмедленных в нашем ощущении времени, циклов. Болезни, возникающие в результате таких эпидемий, целесообразно выделить в новый класс — болезни эндогенной ретровирусной активности .
Для эпидемических процессов, вызываемых эндогенными ретроэлементами, можно выделить следующие стадии:
межзпидемическая стадия — в результате эпидемии (эпизоотии) нециклического типа у части выживших представителей данного вида произошла эндогенизация экзогенного ретровируса;
предэпидемическая стадия — в изолированных, практикующих инбридинг популяциях, по мере размножения особей, носителей нового эндогенного ретровируса, происходит увеличение его копий. Через обратную транскрипцию генерируются новые генетических элементы. В географически обособленных популяциях появляются первые особи с наследуемыми генетическими дефектами;
стадия развития эпидемии — в распространение новых генетических элементов вовлекаются панмиксные популяции вида, что приводит к нарастанию пластичности генома. В результате пролиферации транспозируемых элементов с каждым новым поколением происходит увеличение количества особей вида, страдающих наследственными болезнями;
стадия разгара эпидемии — скорость пролиферации транспозируемых элементов и распространение генетических дефектов в панмиксных популяциях достигают максимума, рост числа гомозиготных носителей мутаций. Из-за чрезмерной пластичности генома возможна гибель панмиксного вида и/или появление его подвидов среди географически обособленных популяций;
стадия угасания пандемии — скорость пролиферации по виду (подвиду) транспозируемых элементов снижается ниже того порогового уровня , когда темпы мутационных замен нуклеотидов делают невозможным существование активно транспозирующихся ретроэлементов. Рост числа гетерозиготных носителей мутантных аллелей;
постэпидемическая стадия — следы былых катастроф генома в виде дефектных и неспособных к транспозиции ретроэлементов.
Разумеется, это идеальная схема, так как виды не появляются «с чистого листа» и наследуют ретроэлементы и генетические дефекты своих предшественников. Оказать какое либо противодействие болезням эндогенной ретровирусной активности вряд ли мы сегодня сможем, но изучать их целесообразно именно как проявление сверхдлительного эпидемического цикла ретроэлементов уже потому, что исследуя динамику этого процесса можно заглянуть в будущее вида H . sapiens .
Использованная литература
• Nelson P. N., Hooley P., Roden D. et al. // Clin. Exp. Immunol. — 2004. — Vol. 138 . — P. 1–9 .
• Katzourakis A., Pereira V., Tristem M. // J. Virol. — 2007. — Vol. 81, № 19. — P. 10712–10717.
• Deininger P., Batzer M. // Genome Res. — 2002. — Vol. 12. — P. 1455—1465.
• Ostertag E. M., Kazazian H. // Annu. Rev. Genet . — 2001. — Vol . 35. — P . 501 – 538.
• Аст Г. // В мире науки. — 2005. — № 7. — С. 37–43.
• Moses A. E., Adelowo K. A., Nwankwo E. A. // Niger Postgrad. Med. J. — 2001. — Vol. 8, № 2. — P. 74 – 77.
Библиографическое описание:
Супотницкий М. В. Болезни эндогенной ретровирусной активности // Энвайронментальная эпидемиология . — 2009. — Том 3, № 2. — С. 151 – 156.
Работа так же была представлена на Всероссийской научно-практической конференции, посвященной 60-летию филиала ФГУ «48 ЦНИИ Минобороны России — ЦВТП БЗ», состоявшейся 16.07.2009 г. в Екатеринбурге.
Супотницкий М. В. Болезни эндогенной ретровирусной активности // Актуальные проблемы биологической защиты войск и населения. Материалы Всероссийской научно-практической конференции, посвященной 60-летию филиала ФГУ «48 ЦНИИ Минобороны России — ЦВТП БЗ». — Екатеринбург, 2009. — С. 196–198.

Михаил Васильевич Супотницкий
Российский микробиолог, полковник медицинской службы запаса, изобретатель, автор книг и статей по истории эпидемий чумы и других особо опасных инфекций, истории разработки и применения химического и биологического оружия. Заместитель главного редактора научно-практического журнала «Вестник войск РХБ защиты» Министерства обороны РФ.
Метки: 2009